新闻中心 / News Center
贝达药业BPI-520105片药品临床试验申请获受理
日期: 2024-01-08
1月5日,贝达药业收到国家药品监督管理局签发的《受理通知书》(受理号:CXHL2400010国;CXHL2400011国;CXHL2400012国),公司申报的BPI-520105片药品临床试验申请已获得国家药品监督管理局受理。
BPI-520105是由公司自主研发的拥有完全自主知识产权的新分子实体化合物,是一种新型强效、高选择性的针对多种EGFR突变的Pan-EGFR抑制剂,拟用于治疗携带EGFR突变的实体瘤患者。
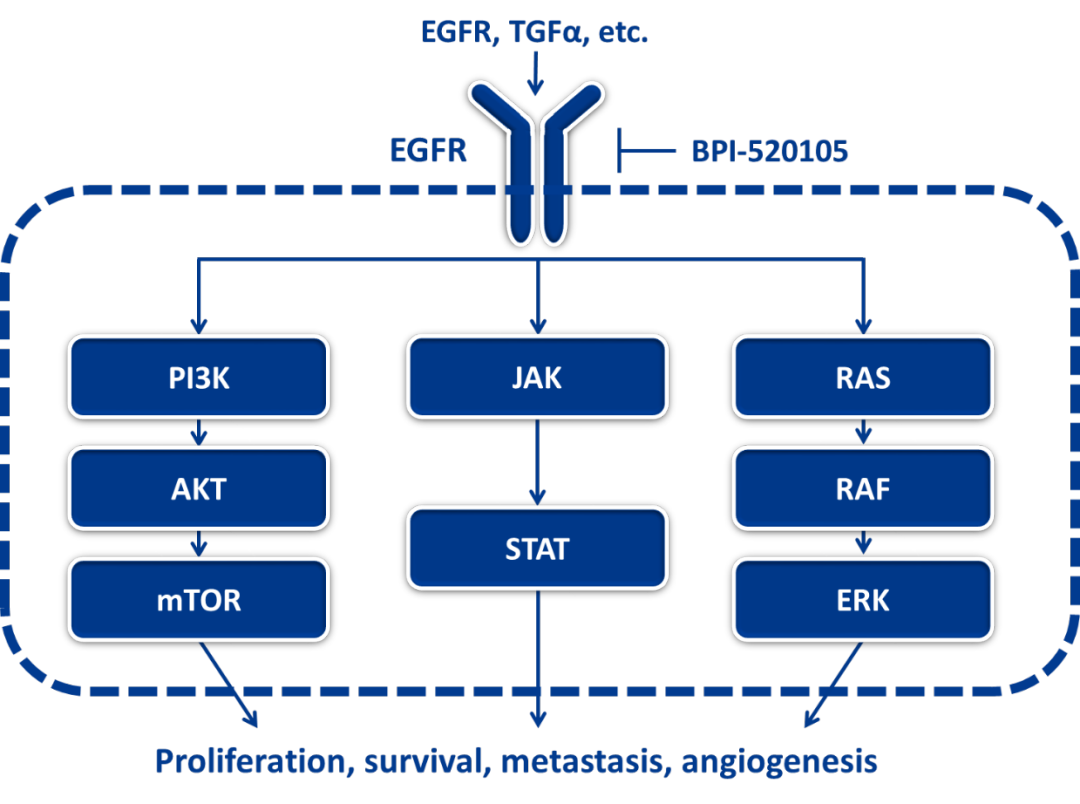
△BPI-520105作用机理图
临床前研究显示,BPI-520105能够高效抑制多种EGFR突变,包括EGFR常见及罕见的单突变、携带T790M和/或C797S的双突变和三突变等。BPI-520105通过抑制EGFR磷酸化及下游信号通路发挥抗肿瘤作用。BPI-520105临床前研究展现出良好的体外及体内活性、药代动力学性质及良好的安全性。
贝达药业资深副总裁兼首席科学家王家炳博士表示,BPI-520105作为一个Pan-EGFR抑制剂,可实现对EGFR突变的全覆盖,在治疗EGFR突变的癌症上可望有广泛的应用前景。
下一条: 贝达药业BPI-221351片药品临床试验申请获受理
热门点击
